Le Parisien via AFP
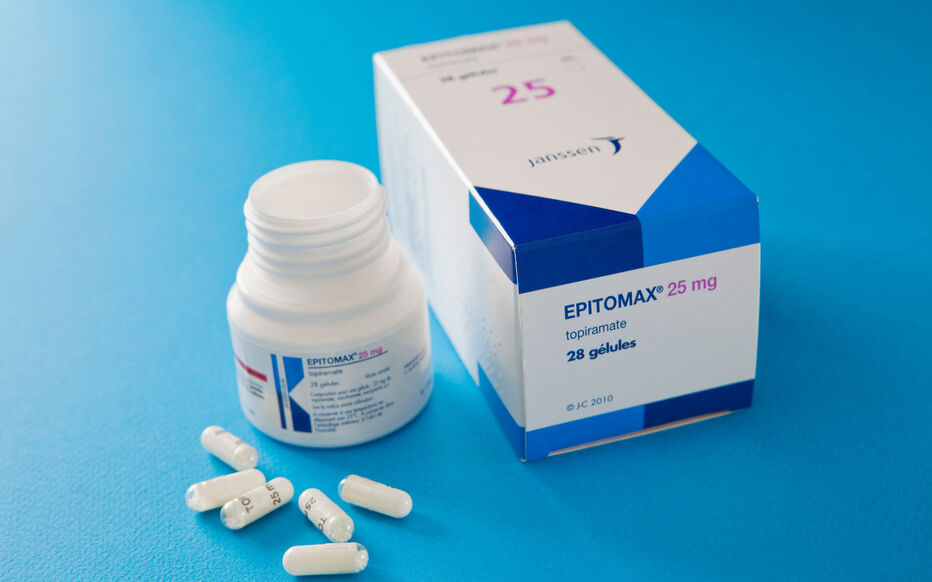
Ce médicament, vendu sous la marque Epitomax par le laboratoire Janssen mais aussi comme générique par d’autres fabricants, est prescrit contre les crises d’épilepsie et les migraines.
L’Agence du médicament (ANSM) annonce ce jeudi des restrictions sur la prescription du topiramate chez les femmes, un antiépileptique à risques pour le fœtus et sous réserve que les patientes signent un consentement. Le topiramate, vendu sous la marque Epitomax par le laboratoire Janssen mais aussi comme générique par d’autres fabricants, est prescrit contre les crises d’épilepsie et les migraines.
En juin, l’ANSM avait déjà rappelé qu’il fallait éviter au maximum sa prescription chez la femme enceinte et chez toute femme susceptible d’attendre un enfant, même de façon imprévue.
Un risque accru de troubles du neurodéveloppement
On sait en effet depuis plusieurs années que le topiramate démultiplie les risques de malformations chez le fœtus. Des études récentes ont aussi mis en évidence un risque accru de troubles du neurodéveloppement pour l’enfant à naître. À compter du 2 novembre, un médicament à base de topiramate ne pourra être prescrit la première fois aux femmes concernées que par un neurologue ou un pédiatre, a annoncé l’ANSM. Lors de cette première prescription, elles devront signer un formulaire attestant qu’elles ont bien été informées des risques pour l’enfant à naître.
La signature d’un accord désormais nécessaire
En cas de traitement déjà commencé, elles devront prendre rendez-vous dès que possible avec un neurologue ou un pédiatre d’ici à mai prochain, pour éventuellement renouveler la prescription et signer leur accord. « Pour les patientes traitées pour une épilepsie, il ne faut surtout pas qu’elles arrêtent subitement le traitement sans en avoir parlé à leur médecin », prévient Philippe Vella, directeur médical au sein de l’ANSM
Côté pharmaciens, pour toute dispensation du médicament, la présentation de la prescription initiale annuelle du spécialiste en neurologie ou en pédiatrie ainsi que le formulaire annuel d’accord de soins cosigné, sera obligatoire à compter du 2 novembre pour démarrer le traitement, et du 2 mai pour les patientes en cours de traitement.
« Sauf en cas de nécessité absolue »
Au vu des dernières études, l’ANSM a demandé à son homologue européenne, l’Agence européenne du médicament (EMA), de réévaluer les conditions de prescription du topiramate.
Chez les femmes enceintes ou les femmes en âge d’avoir des enfants et qui ne disposent pas d’une méthode de contraception efficace, le topiramate est contre-indiqué dans le traitement de la migraine et dans le traitement de l’épilepsie, sauf en cas de nécessité absolue, rappelle-t-elle.





